当然,信息还是以官方公布为准!本文仅供参考、思考。
报量的重要性不言而喻
关于报量的重要性,我们在之前的文章集采“四连环”:报量-报价-市场选择-标后攻防,通盘考量,统一规划中已经为你分析过,报量是集采从制度到政策到实施后的第一起点,不仅影响医院后期的遴选、使用,还关系其能否兑现结余留用政策。
当然,很多企业也在积极行动,目录,不是还未正式公布吗?不是还有汇总、调整、完善的空间吗?一切不都是各方达成共识的结果吗?
第五批未纳入中成药、生物类似药
此次网传报量目录60个品种,207个品规,是从2018年4+7集采以来历次纳入品种最多的一次,且有30个注射剂,真正进入了注射剂时代和重磅品种集采时代。
不过,此次还未涉及业界高度关注的中成药和生物制品,这两类药品相对化学药而言标准化程度较低,如何分类(拆分或合并),按适应症/功能主治?还是考虑某些品种兼具药物+耗材+服务属性?这都是集采的难点之一。
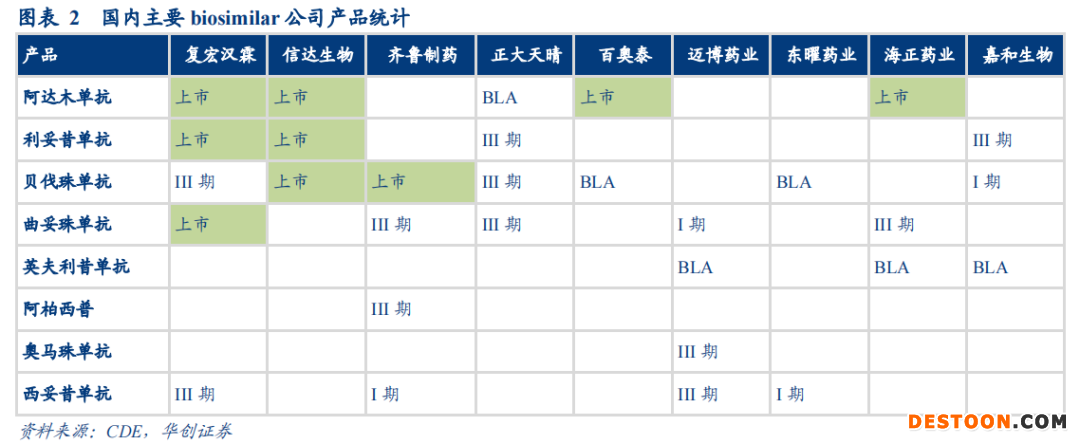
此外,对于生物类似药而言,从2019年国内才有第一个品种出现,虽然至今阿达木单抗、贝伐珠单抗、利妥昔单抗都到达或超过3家,满足集采的“触发机制”,但这一领域几个玩家,如齐鲁、复宏汉霖、海正、信达、百奥泰创业不易,商业化不易,是否应该全盘考虑选择一种较为稳妥的方式推进?
集采的触发机制是?
按国办发[2021]2号文及国家医保局相关负责人的表态,中成药、生物类似药不存在集采禁区,且“纳入集采毫无疑义”,“基本上是采取原研药加通过一致性评价的仿制药,只要达到三家就可以列入集采”。”
截至2021年4月14日,医药云端工作室统计满足“原研+过评达到或超过三家”的品种达到82个。而此次报量目录显示60个品种,那么,剩下的22个品种为何没有纳入到集采?其中不乏临床使用成熟、采购金额超大的某PPI。
显然,我们认为,所谓的“触发机制”还需要在具体品种中具体评估,产品特殊性、产能、质量风险、用药风险、使用方式等因素不得不全面考虑。
近日,旗帜网发表国家医保局负责同志的署名文章《由构建医药价格治理新格局》,为下一步集采工作中进行分类提出了很有建设性、创建性的思路,值得业界好好品味。
文章指出,要不断完善和发展集中带量采购综合运用采购量、合约期、竞争度、替代性不断创新集中采购工具箱。
对普适性较强的品种按统一规则集中采购
对高值医用耗材按“一品一策”推进
对特征性较强的品种探索专项集中采购
对适应症和功能主治相似的品种探索合并集中采购
对供求关系变化较大的探索分阶段议价采购
从上述几条思路可以看出,第五批集采品种依然属于“普适性较强的品种”,因此按照从第三批开始逐渐成熟的规则来集采。
而高值耗材从第一批开始,虽然只有一个品种---冠脉支架的集采思路就显得很格局开阔,规则制定很娴熟,既尊重了医疗机构的使用品种、采购量,又提供了开放的准入之门充分竞争,于是实现了历史性的降价。照此思路,第二批骨关节耗材集采也将“一品一策”。
而对于特征性较强的品种、适应症或功能主治相似的品种、供求关系变化较大的品种,则结合产品特点采用不同方式“探索”,可能会从国家、地方层面推开。



