CRC(clinical research coordinator,临床研究协调员)作为研究团队一员,指经PI授权,并接受相关培训后,在临床试验中协助研究者从事非医学判断相关工作的人员,是临床试验的执行者和协调者。
别说在校的大学生没有听说过“临床协调员”这个职位,很多医院的护士都不知道她们究竟是怎么样的一个存在,更不清楚它有多大的发展前景和潜力。
今天我们就来聊一聊CRC到底是什么?
70年代,欧、美、日等发达国家把CRC作为药物临床试验的重要参与者,最初由护士兼任,后来慢慢培养出专业的CRC团队。
我国自2003年9月1日《药物临床试验质量管理规范》实施以来,对临床试验中的各个方面都提出了具体的要求,包括伦理、研究人员职责和效率等。在药物临床试验日趋规范的背景下,CRC职业应运而生,它解决了研究者因医务工作繁忙,无法及时完成药物临床试验中很多繁琐的事务性工作问题。CRC最初由护士兼任,后来发展到自由职业者担任,直至2004年国内终于出现了专业的SMO团队。
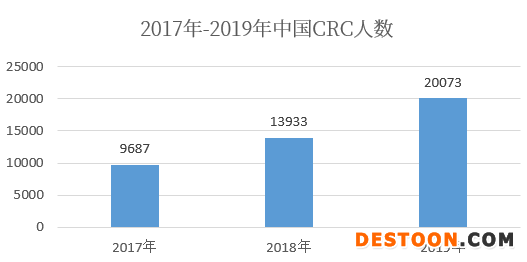
近年来,随着国内临床试验机构数量的不断增加,医药外包行业更是迎来了蓬勃发展期,CRC从业者由2017年的9687人增长到2019年的20073人,医院机构也开始建立自己的CRC团队。
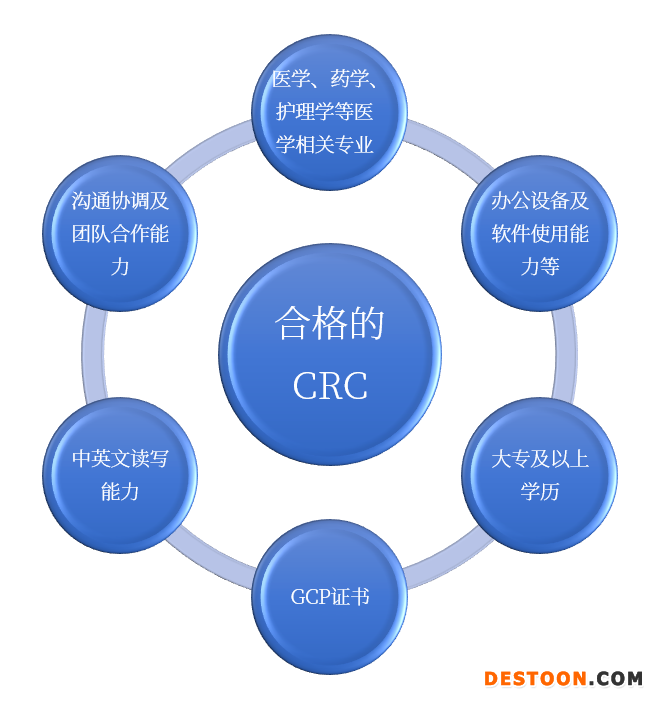
03 CRC的工作职责
试验启动前:
-
协助准备研究者的资质文件,如个人简历、培训证书GCP证书、执业医师资格证书和执业护士资格证书;
-
收集相关检查设备校准证书、实验室检查项目正常值范围及室间质评证书;
-
协助调研科室和机构的备案资质;
-
协助研究者完成立项/伦理委员会/合同审核申请等事务性工作;
-
研究物资及研究药物的接收;
-
联系协调相关科室与人员参加临床研究项目启动会;
-
完成试验相关的其他工作。
试验进行中:
-
协助研究者进行受试者招募;
-
协助研究者对受试者进行知情同意,协助筛选受试者,核对入排标准;
-
联系研究者与受试者,安排受试者来院访视,提前做好受试者访视的准备工作;
-
合理安排受试者访视各项工作;
-
协助研究者记录不良事件及合并用药等;
-
管理临床研究相关文档,协助伦理文件递交与取回;
-
在PI授权范围内,协助药品管理员管理研究药物;
-
协助收集血样,离心处理血样和联系冷链快递血样到中心实验室,但不得进行抽血、注射和其他未经授权的医学操作;
-
根据原始记录,及时、准确录入EDC;
-
协助研究者进行不良事件与严重不良事件的报告,但不得进行医学判断和医学处置;
-
协助研究者进行内部和外部的沟通联系;
-
协助监查员对试验项目进行监查,配合稽查、视察等;
-
协助完成研究者授权的其他工作。
试验结束:
-
协助研究者对eCRF的质疑进行合理回复;
-
整理研究者文件及原始病历等资料,协助机构人员进行文件保存与归档;
-
完成研究者授权的其他工作;
-
协助中心关闭工作。
CRC其实与医护人员有着同样的信仰和职业操守。应遵循GCP法规,赫尔辛基宣言,并宣读希波克拉底誓词。因为CRC的工作关系到整个临床试验结果的真实性和可靠性,关系到患者用药安全和疗效。
为规范专业化CRC的工作,SMO公司和研究机构建立了对CRC的管理制度,对CRC进行监督管理、工作考评和专业培训。CRC应严格按照PI授权开展职责范围内的工作,并服从研究机构的管理。如果出现下列行为之一,研究机构可采取相应的处罚措施,情节严重,造成受试者伤害事件或严重影响数据真实可靠性的,由CRC承担法律责任。
-
违反研究机构制度规定;
-
违背临床试验方案;
-
故意伪造或篡改研究数据;
-
擅自从事授权之外的医疗护理相关工作;
-
泄露申办者、受试者及研究机构相关信息;
-
违背本行业指南要求的行为准则,出现严重后果。
实践表明,CRC参与临床研究后,均能严格按照GCP相关要求和法律法规执行,严格遵循试验方案及各项标准操作规程,保证了临床试验过程规范、结果科学可靠。不仅推动了项目的进度,同时提高了研究质量,大大减轻了研究者的事务性工作的压力。
由于CRC这一职业在中国出现相对较晚,它随着临床研究工作的成熟,逐渐独立出来,目前行业内至少存在2万CRC缺口,这对于从业者来说,相对利好,现在也是进入临床行业的最佳时期。
新人成为CRC,首先有一个打基础的阶段,一般需要1年~2年时间,对各种事务性工作进行熟悉,处理病人访视,归档研究文件等等。
当CRC积累1~2年从业经验后可升为二级CRC,也可转行做CRA(临床监查员)、临床质控员(QC)等。随着项目经验的积累和优的工作表现,可晋升为高级CRC1和高级CRC2。当经验和管理能力达到可统筹项目的水平时,可晋升项目经理或其他管理人员。
总之,职业发展后期的选择面会越来越宽,大家可以根据自己的兴趣、性格来进行职业规划。晋升不止看从业年限,还要考察专业水平和业务素质,没有不劳而获的升职。加油吧!打工人!
-END-
关于我们:
北京济美堂医药研究有限公司成立于2012年,是北京新领先的长期合作伙伴,拥有近200人的CRC团队,分布在全国多个主要城市,并在北京、石家庄、郑州、杭州、长沙、武汉等主要城市设立了众多办事处。
公司CRC团队均为护理或药学专业毕业,多数拥有本科及以上学历,并拥有丰富的BE、大临床、器械项目经验。公司致力于通过提供临床试验相关的专业服务,协助研究机构研究者、申办方和CRO承担在临床试验中非医学判断的工作,保证临床试验质量和推进临床试验进度,保证临床试验规范化进程。





